The bioavailability and pharmacokinetics of glucosamine hydrochloride and low molecular weight chondroitin sulfate after single and multiple doses to beagle dogs. (Biodisponibilité et pharmacocinétique du chlorhydrate de glucosamine et du sulfate de chondroïtine après une ou plusieurs doses administrées à des chiens de race beagle). Biopharm. Drug Dispos. 23 (66): 217-225 Objectif: Le but de cette étude était de déterminer la biodisponibilité et la pharmacocinétique du chlorhydrate de glucosamine et du sulfate de chondroïtine après une ou plusieurs administrations de Cosequin® DS chez le chien.Méthode: Huit chiens beagle ont été utilisés pour déterminer la biodisponibilité dans un test croisé randomisé avec 3 séries. Une semaine séparait chaque série.
Les 3 groupes de traitement par voie orale en dose unique étaient:
(1) 500 mg de glucosamine HCl et 400 mg de sulfate de chondroïtine (1 gélule de Cosequin® DS),
(2) 1500 mg de glucosamine HCl et 1200 mg de sulfate de chondroïtine (3 gélules de Cosequin® DS)
(3) 2000 mg de glucosamine HCl et 1600 mg de sulfate de chondroïtine (4 gélules de Cosequin® DS).Par ailleurs, pour déterminer la pharmacocinétique des deux composés, tous les chiens reçurent 1500 mg de glucosamine HCl et 1200 mg de sulfate de chondroïtine (3 gélules de Cosequin® DS) par voie orale pendant 7 jours. La concentration plasmatique de la chondroïtine sulfate a été déterminée par la somme de ses trois métabolites principaux (Di-OS, Di-4S, Di-6S)Résultats: La glucosamine HCl est rapidement absorbée avec un Tmax d’une heure et trente minutes. Le sulfate de chondroïtine est aussi rapidement absorbé avec un Tmax de 2 heures. Les biodisponibilités du sulfate de chondroïtine et de la glucosamine ont été de 5% et 12% respectivement après une dose unique. Un effet cumulatif a été demontré après administrations répétées, et une biodisponibilité de 200% a été calculée après 7 jours.
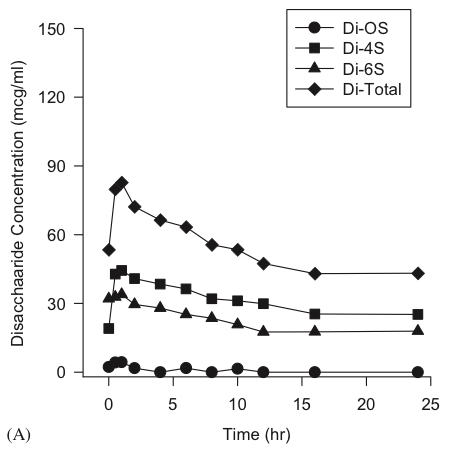
Conclusion: Cette étude démontre la biodisponibilité de la glucosamine HCl et du sulfate de chondroïtine de faible poids moléculaire après administration de Cosequin® DS par voie orale. Le sulfate de chondroïtine montre un effet cumulatif après plusieurs jours de traitement (voir graphe ci-dessus.)
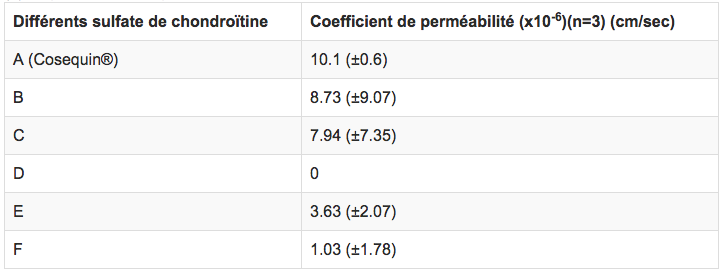
Analysis of glucosamine and chondroitin sulfate in marketed products and the Caco-2 permeability of chondroitin sulfate raw materials. (Analyse de la quantité de glucosamine et de chondroïtine sulfate contenue dans des produits sur le marché et la perméabilité des cellules Caco-2 au sulfate de chondroïtine brut.) Journal of the American Nutraceutical Association 3(1): 37-44.La quantité de glucosamine et de sulfate de chondroïtine contenue dans plusieurs produits sur le marché a été analysée dans cette étude par une méthode UV-HPLC.84% des produits ne contenaient pas la quantité indiquée sur l’étiquette avec des valeurs allant de 0 à 115% de celles des étiquettes, certains produits ne contenant que 10% de ces quantités.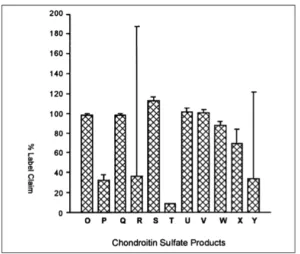 La capacité de plusieurs sulfates de chondroïtine de différentes origines à être absorbée au niveau du tube digestif a été évaluée à l’aide d’un test mesurant la perméabilité à travers une couche de cellules Caco-2. Les coefficients de perméabilité calculés à partir de ce test allaient de 10.1 pour Cosequin® à 0, certains produits n’étant pas absorbés du tout.Cette analyse démontre :(1) une grande variabilité dans l’absorption des chondroïtines, et donc de leur biodisponibilité potentielle,
La capacité de plusieurs sulfates de chondroïtine de différentes origines à être absorbée au niveau du tube digestif a été évaluée à l’aide d’un test mesurant la perméabilité à travers une couche de cellules Caco-2. Les coefficients de perméabilité calculés à partir de ce test allaient de 10.1 pour Cosequin® à 0, certains produits n’étant pas absorbés du tout.Cette analyse démontre :(1) une grande variabilité dans l’absorption des chondroïtines, et donc de leur biodisponibilité potentielle,
(2) la qualité de Cosequin®.
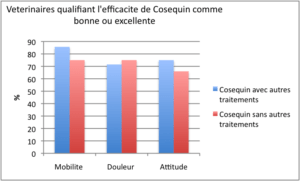
Results of a survey of small-animal practitioners on the perceived clinical efficacy and safety of an oral nutraceutical. (Résultats d’un sondage auprès de vétérinaires spécialistes des animaux de compagnie sur leur perception de l’efficacité et de la toxicité d’un aliment complémentaire).Preventive Veterinary medicine 38: 65-73.3080 vétérinaires furent sondés par courrier sur l’efficacité de Cosequin® durant les 6 mois précédant le sondage. Les vétérinaires ont estimé avoir traité 28898 chiens avec des problèmes articulaires durant cette période. L’articulation la plus souvent affectée est celle de la hanche suivie par le grasset, le coude, l’épaule et le jarret. 46% des vétérinaires utilisent Cosequin® comme traitement principal. 59% utilisent Cosequin® en association avec d’autres agents comme les AINSs, la majorité d’entre eux indiquant que l’usage de ces agents est réduit ou même éliminé avec le temps et Cosequin®.Les vétérinaires indiquent que Cosequin® est bon à excellent pour réduire la douleur, améliorer la mobilité et le bien-être pour 80% des animaux recevant ce produit. Des effets secondaires furent observés dans moins de 2% des animaux sous la forme de troubles digestifs mineurs.
Further studies on the ability of glucosamine and chondroitin sulphate to regulate catabolic mediators in vitro. (Etudes sur la capacité de la glucosamine et du sulfate de chondroïtine à moduler les médiateurs du catabolisme in vitro). Equine Veterinary Journal 36 (7): 634-636.Des fragments de cartilage articulaire de cheval ont été mis en culture in vitro et stimulés à l’aide de lipopolysaccharide (LPS). L’addition de glucosamine HCL et de sulfate de chondroitin (Cosequin®) a inhibé la production de médiateurs inflammatoires (oxyde nitrique NO et prostaglandine E2 ) et diminué l’activité de l’enzyme protéolytique MMP-9. Cette étude apporte la preuve que l’association glucosamine HCL et sulfate de chondroïtine contenue dans Cosequin® protège le cartilage de la dégradation.
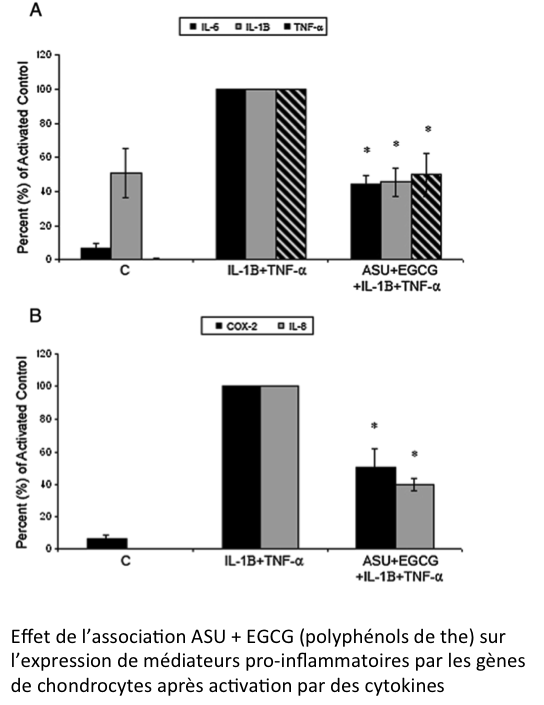
Expression of pro-inflammatory mediators is inhibited by an avocado/soybean unsaponifiable and epigallocatechin gallate combination. (L’expression de médiateurs pro-inflammatoires est inhibée par une association d’ insaponifiables avocat/soja et d’épigallocathéchine-3-gallate). Journal of Inflammation 11:8. Des chondrocytes de chevaux adultes provenant de l’articulation du carpe ont été incubés in vitro pendant 24 heures soit avec un placebo soit avec une association d’insaponifiables avocat soja (ASU) et d’épigallocathéchine-3-gallate (EGCG ou polyphénols de thé) suivi par une activation pendant une heure avec de l’interleukine-1-beta (IL-1 β) et de facteur nécrosant des tumeurs-alpha (TNF-α). ASU+ EGCG contenu dans Cosequin® Equin ASU+HA inhibent l’expression de gène encodant pour IL-1β, TNF-α, IL-6, COX-2 et IL-8 après stimulation des chondrocytes par des cytokines. Cette inhibition est liée à une modulation du facteur Nf-kB, un régulateur de plusieurs gènes codant pour des protéines de l’inflammation.
En plus de la diminution de la synthèse de PGE2 par des chondrocytes activés, l’association ASU+EGCG contenue dans Cosequin® Equin ASU+HA contrôle un grand nombre de médiateurs pro-inflammatoires impliqués dans l’ostéoarthrite ce qui valide leur utilisation pour améliorer le confort et la mobilité des chevaux.
Des fragments de cartilage articulaire de cheval ont été mis en culture in vitro et stimulés à l’aide de lipopolysaccharide (LPS). La glucosamine HCL et le sulfate de chondroïtine contenus dans Cosequin® agissent en synergie pour diminuer la dégradation induite par LPS, un médiateur de l’inflammation. L’expression de métalloprotéinase -9 (MMP-9) et la production de prostaglandine E2 ont été diminuées par l’association de 1mg/ml de glucosamine HCL et 0.25 mg/ml de chondroïtine sulfate. Les auteurs concluent que la glucosamine HCL et le sulfate de chondroïtine contenus dans Cosequin® se complètent pour diminuer la dégradation du cartilage.

Cartilage stimulatory and antiproteolytic activity is present in sera of dogs treated with a chondroprotective agent. (Une activité anabolique et antiprotéolytique du cartilage est présente dans le sérum de chiens traités avec un chondroprotecteur). Canine Practice 24 (1): 18-19. Des sérums de chiens en bonne santé ont été collectés avant et après administration de Cosequin® pendant 30 jours. Au jour 30 le taux de glycosaminoglycanes (GAG) dans la sérum a augmenté de façon significative (+42%). Ces sérums ont été aussi incubés avec des fragments de cartilage. Le taux de biosynthèse des glycosaminoglycanes par le cartilage a augmenté de façon significative (+ 50%). De plus, une réduction significative de l’activité protéolytique a été observée (-59%). Les auteurs concluent que Cosequin® administré oralement pendant une longue période augmente la concentration sanguine d’agents qui stimulent le métabolisme du cartilage et inhibent la dégradation du cartilage.
In vivo chondroprotection and metabolic synergy of glucosamine and chondroitin sulfate. Clin. Orthop. Relat. Res. 381: 229-240. Chondroprotection in vivo et synergie métabolique après administration de glucosamine et sulfate de chondroïtine seul ou en association.
Objectif: Evaluer si la glucosamine HCL, le sulfate de chondroïtine et le sulfate de manganèse ou l’association des trois (Cosequin®DS) retarde la dégénérescence du cartilage articulaire dans un modèle animal d’ostéoarthrite.
Méthode : Une instabilité du genou a été créée par résection des ligaments croisés antérieurs et postérieurs sur 42 lapins de race New Zealand White. Trois jours après la chirurgie 2 groupes de 12 animaux furent traités avec (1) une nourriture standard ou (2) une nourriture standard plus Cosequin® DS (500mg de glucosamine HCL, 400 mg de sulfate de chondroïtine de faible poids moléculaire et 76 mg d’ascorbate de manganèse). Trois groupes de 6 animaux ont reçu la nourriture standard plus soit (3) de la glucosamine HCL, (4) du sulfate de chondroïtine ou (5) de l’ascorbate de manganèse. Tous les animaux furent traités pendant 16 semaines. La sévérité et l’étendue des lésions ont été mesurées par examen de coupes histologiques du condyle fémoral interne colorées à la safranine O.
Résultats : Aucun des animaux du groupe traité avec Cosequin®DS n’a montré de signes sévères de lésions du cartilage comparé à 83% des animaux du groupe contrôle. La sévérité des lésions a aussi été réduite de façon significative pour le groupe traité avec Cosequin®DS par rapport au groupe contrôle (59% et 74% respectivement). Les groupes traités avec les composants administrés séparément n’ont pas montré de différence par rapport au groupe contrôle. Microphotographies de coupes du condyle fémoral interne. Le colorant à la safranine O a coloré la glycosaminoglycane dans la matrice cartilagineuse. Noter la perte de la couche de cartilage dans le groupe contrôle. Conclusions : L’association de glucosamine HCL, de sulfate de chondroïtine et d’ascorbate de manganèse (Cosequin®DS) a réduit de façon significative la progression de la dégénérescence du cartilage. L’effet de l’association des 3 composants a été supérieur à celui de chaque composant pris séparément.
Conclusions : L’association de glucosamine HCL, de sulfate de chondroïtine et d’ascorbate de manganèse (Cosequin®DS) a réduit de façon significative la progression de la dégénérescence du cartilage. L’effet de l’association des 3 composants a été supérieur à celui de chaque composant pris séparément.
Heinecke LF, Grzanna MW, Au AY et al 2010. Inhibition of cyclooxygenase-2 expression and prostaglandin E2 production in chondrocytes by avocado soybean unsaponifiables and epigallocathecin gallate. (Inhibition de l’expression de cyclooxygénase-2 et de la production de prostaglandine E2 dans des chondrocytes par les fractions insaponifiables d’avocat et de soja et l’épigallocathécine gallate). Osteoarthritis and Cartilage 18 : 220-227.Des chondrocytes de chevaux adultes provenant de l’articulation du carpe ont été incubés in vitro pendant 24 heures soit avec un placebo soit avec différentes doses d’insaponifiables avocat soja (ASU), différentes doses d’épigallocathéchine-3-gallate (EGCG ou polyphénols de thé) ou l’association d’ASU et de EGCG, puis est intervenue une incubation avec de l’interleukine-1-beta (IL-1 β) et des facteurs nécrosants des tumeurs-alpha (TNF-α). ASU et EGCG sont des composants de Cosequin® Equin ASU + HA.Les chondrocytes équins répondent à l’activation par les cytokines IL-1β et TNF-α par une up- régulation du gène encodant pour la cyclooxygénase -2 (COX-2) et une augmentation de la production de prostaglandine E2 (PGE2). Individuellement l’ASU et la EGCG inhibent l’expression de COX-2 et la production de PGE2 de façon marginale. En revanche l’association ASU + EGCG réduit l’expression des COX-2 au niveau de celui obtenu sans activation ainsi que la production de PGE2 de façon statistiquement significative.

COX-2 dans des chondrocytes en culture activés par des cytokines.
Cette étude démontre l’effet synergique d’ASU et EGCG sur l’inflammation lorsqu’ils sont employés ensemble. Les auteurs considèrent que cette association est une alternative aux anti-inflammatoires non stéroïdiens.
Oral treatment with a glucosamine-chondroitin sulfate compound for degenerative joint disease in horses: 25 cases. (Traitement par voie orale avec un produit associant la glucosamine au chondroïtine sulfate des maladies dégénératives articulaires du cheval: 25 cas). Equine Practice. 19(9) : 16-22.25 chevaux présentant des signes de maladies dégénératives articulaires confirmés par radiographie ou fluoroscopie au niveau du jarret, genou ou paturon ont été traités par voie orale avec Cosequin® pendant 6 semaines. Tous les 15 jours les chevaux ont été examinés et un score de boiterie, flexibilité et longueur de la foulée ont été déterminés.Pour tous les paramètres mesurés une amélioration rapide a été observée, et cette amélioration continue pendant les 6 semaines. L’amélioration est indépendante de l’âge, de l’articulation et de l’utilisation du cheval. Certains chevaux ont été capables de retourner à la compétition après seulement 2 semaines de traitement.
Oral treatment with a nutraceutical (Cosequin®) for ameliorating signs of navicular syndrome in horses. (Traitement par voie orale avec un nutraceutique (Cosequin®) pour améliorer les symptômes de maladie naviculaire chez le cheval). Veterinary Therapeutics. 2 (2) : 148-159.14 chevaux âgés de 5 à 15 ans avec un historique de boiteries progressives des membres antérieurs classées comme maladies naviculaires ont été répartis au hasard dans 2 groupes traités pendant 8 semaines, soit avec Cosequin® à la dose recommandée par le fabriquant, soit avec un placebo. L’étude a été conduite en double aveugle, le clinicien et les propriétaires des chevaux ne connaissaient pas le traitement administré.La sévérité des boiteries était déterminée par un index calculé à partir d’une évaluation au repos et en mouvement et d’un examen du sabot par le clinicien. L’état général des chevaux était évalué à partir d’une échelle VAS par ce même clinicien lors de l’enrôlement du cheval dans l’étude et après 4 et 8 semaines. Les propriétaires devaient aussi évaluer les boiteries à partir d’un questionnaire à remplir chaque semaine.La sévérité des boiteries a été réduite de façon significative par le traitement avec Cosequin® (p=0.05). De plus l’état général des animaux était aussi meilleure (p=0.02). Les propriétaires ont eux aussi noté une amélioration significative après 8 semaines de traitement (p=0.045).Les auteurs de l’étude concluent que Cosequin® est efficace pour cette indication.
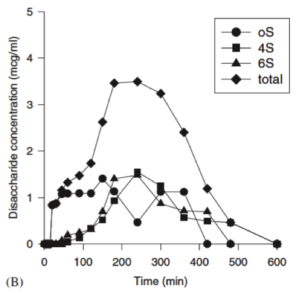
The bioavailability and pharmacokinetics of glucosamine hydrochloride and chondroitin sulfate after oral and intravenous single dose administration in the horse. (La biodisponibilité et la pharmacocinétique de la glucosamine HCL et du sulfate de chondroïtine après administration d’une dose par voie orale ou intraveineuse chez le cheval. Biopharmaceutics & Drug Disposition 25: 109-116.Le but de cette étude était de déterminer si la glucosamine HCL (FCHG49®) et le sulfate de chondroïtine (TRH122™) contenus dans Cosequin® sont absorbés après administration par voie orale. La biodisponibilité du sulfate de chondroïtine de faible poids moléculaire a été déterminée par mesure des disaccharides totaux contenus dans le plasma après digestion par la chondrotinase ABC. Le sulfate de chondroïtine de faible poids moléculaire (16.9kD) est absorbé rapidement (TMAX 1.3 heures) avec une biodisponibilité estimée à 22%. La glucosamine HCL est aussi rapidement absorbée (TMAX 2 heures) avec une biodisponibilité estimée à 2.5 %. Cette étude est la seule apportant une preuve de l’absorption de la chondroïtine chez le cheval.
Effects of glucosamine and chondroitin sulphate, alone and in combination, on normal and interleukin-1 conditioned articular cartilage explant metabolism. (Effets de la glucosamine et du sulfate de chondroïtine, seuls ou en association, sur le métabolisme de fragments de cartilage normaux ou prétraités avec l’interleukine-1). Equine veterinary Journal 37(3) : 227-231.Des fragments de cartilage articulaire de cheval ont été mis en culture in vitro et stimulés à l’aide d’ interleukine-1 (IL-1). Aucun effet négatif n’a été observé avec la glucosamine (GU) et le sulfate de chondroïtine (CS), seuls ou en association sur le métabolisme du cartilage normal. L’association de glucosamine HCL et de sulfate de chondroïtine contenus dans Cosequin® diminue le relargage de glycosaminoglycane (GAG) induit par l’IL-1 dans le milieu de culture, un indicateur de dégradation de cartilage. GU et CS seuls n’ont pas le même effet.Les auteurs concluent que pour la protection du cartilage un meilleur effet bénéfique est observé avec l’association GU + CS de Cosequin qu’avec GU et CS employés seuls.
Scintigraphic evaluation of dogs with acute synovitis after treatment with glucosamine hydrochloride and chondroitin sulfate. (Examen par scintigraphie de chiens affectés de synovite après traitement au chlorhydrate de glucosamine et sulfate de chondroïtine.) Am. J. Vet. Res. 660 (12) : 1552-1557.
Objectif : Evaluer les effets d’un traitement par voie orale d’une association chondroïtine sulfate+glucosamine HCL (Cosequin® DS) sur une synovite aiguë induite chimiquement.
Méthode : 32 chiens en bonne santé ont été repartis en 4 groupes de traitement (8 chiens par groupe) dans une étude en double aveugle avec contrôle par placebo. Les traitements ont été administrés pendant les 21 jours précédant l’induction de synovite par injection de chymopapaïne dans l’articulation du carpe. L’inflammation a été mesurée par scintigraphie.
Résultats : L’évaluation révèle une réduction de l’inflammation au jour 48 pour le groupe traité par rapport au groupe placebo, illustrée par une réduction significative de l’activité scintigraphique au niveau des tissus mous (4 jours) et de l’absorption par l’os. De plus les scores pour mesurer la boiterie étaient réduits de façon significative pour le groupe traité avec Cosequin® DS par comparaison avec le placebo aux jours 12 à 19, 23 et 24 après l’induction de synovite.
De plus les scores pour mesurer la boiterie étaient réduits de façon significative pour le groupe traité avec Cosequin® DS par comparaison avec le placebo aux jours 12 à 19, 23 et 24 après l’induction de synovite.
Conclusion. Le traitement avec Cosequin® DS pendant 21 jours a un effet protecteur contre une synovite induite chimiquement et le remodelage de l’os qui en résulte. Les boiteries furent aussi améliorées par le traitement.
- Au RY, Phan PV, Au AY, Frondoza CG. Proceedings . 33rd Annual Conference Veterinary Orthopedic Society 2006 ; 75.
- Au R, Phan P, Au A, Frondoza CG. 6th ICRS Symposium 2006 ; poster.
- Beale BS, Hulse DA, Schulz KS, Whitney WO. In: Small Animal Arthroscopy. 1st ed.Philadelphia: WB Saunders Co., 2003, pp.212-223.
- Beren J, Hill SL, Diener-West M, Rose NR. Exper Biol and Med 2001 ; 226 : 144-151.
- Boileau C, Martel-Pelletier J et al. Arthritis Research & Therapy, 2009, 11:R41
- Boothe D, moderator. Vet Forum 2004 ; 20(5A) : 1-12.
- Boulton EP, moderator. Compend Cont Educ Pract Vet 2005 ; 27(5A) : 1-12.
- Cake MA, Read RA et al. Osteoarthritis and Cartilage 2000 ; 8, 404-411.
- Chan PS, Caron JP, Orth MW. Am J Vet Res 2007 ; 68(7) : 709-715.
- Orth MW. J of Rheumatol 2006 ; 33(7) : 1329-1340.
- Chan PS, Caron JP, Rosa GJM, Orth MW. Osteoarthritis Cartilage 2005 ; 13(5) : 387-394.
- Chan PS, Caron JP, Orth MW. Am J Vet Res 2005 ; 66(11) : 1870-1876.
- Clegg DO, Reda DJ, Harris CL, et al. N Engl J Med 2006 ; 354(8) : 795-808.
- Das A Jr, Hammad TA. Osteoarthritis Cartilage 2000 ; 8(5) : 343-350.
- Davidson G. Comp Contin Educ Pract Vet 2000 ; 22(5) : 454-458.
- Demko JL, Phan PV, Kramer EA, et al. Proceedings . 34th Annual Conference Veterinary Orthopedic Society 2007 ; 25.
- Frondoza CG, Heinecke L, Grzanna MW, et al. ICRS 2009 – 8th World Congress of the International Cartilage Repair Society ; P59.
- Gabay O, Gosset B, et al. Osteoarthrisis and Cartilage 2008 ; 16, 373-384
- Gluszko P, Stasiek M, Reumatologia 2016 ; 54, 5 : 217-226
- Goetz P, Phytothérapie 2005 ; 5 : 208-210
- Grande D, O’Grady C, Garone E, et al. Osteoarthritis Cartilage 2000 ; 8(Suppl B) : S34-S35.
- Grzanna MW, Heinecke LF, Au AY, et al. 36th Annual Conference Veterinary Orthopedic Society 2009 ; poster.
- Guastella DB, Cook JL, Kuroki K, et al. Proceedings . 32nd Annual Conference Veterinary Orthopedic Society 2005 ; 5.
- Harlan RS, Chan PS, Caron JP, et al. J Anim Sci 2006 ; 84 (Suppl 1):329.
- Heinecke L, Grzanna M, Au A, et al. ICRS 2009 – 8th World Congress of the International – Cartilage Repair Society ; P78.
- Henrotin Y, Marty M, Mobasheri A, Maturita 2014 ; 78 : 184-187
- Hochberg MC, Martel-Pelletier J, Monfort J, et al ; Ann Rheum Dis 2015, 0 : 1-8
- Hochberg MC, Martel-Pelletier J, Monfort J, et al ; Ann Rheum Dis 2016, 75 : 37-44
- Hoffman AR. Compen Contin Educ Pract Vet 2001 ; 23(10) : 888-894.
- Homandberg GA, Guo D, Ray LM. Osteoarthritis Cartilage 2006 ; 14 : 793-806.
- Hulse DS, Hart D, Slatter M, Beale BS. Proceedings . 25th Annual Conference Veterinary , Orthopedic Society 1998 ; 64.
- Hungerford MS, Valaik D. Foot and Ankle Clin of North Am 2003 ; 8 : 201-219.
- Hungerford D, Apple D, moderators. Ortho Today 2003 ; June(Suppl) : 1-15.
- Johnson KA, Hulse DA, Hart RC, et al. Osteoarthritis Cartilage 2001 ; 9(1) : 14-21.
- Kettenacker RW, Griffin D. 2007 AAVPT 15th Biennial Symposium; poster.
- Kirker-Head CA, Kirker-Head RP. Vet Therapeutics 2001 ; 2(4) : 345-353.
- Leffler CT, Philippi AF, Leffler SG, et al. Mil Med 1999 ; 164(2) : 85-91.
- Liang Z, Bonneville C, Senez T, Henderson T. J Pharm Biomed Anal 2002 ; 28 : 245-249.
- Liang Z, Leslie J, Adebowale A, et al. J Pharm Biomed Anal 1999 ; 20 : 807-814.
- Lippiello L, Nardo JV, Harlan R, et al. Evid Based Complement Alternat Med 2008 ; 5(2) : 191-197.
- Lippiello L. Evid Based Complement Alternat Med 2007 ; 4(2) : 219-224.
- Lippiello L. Osteoarthritis Cartilage 2003 ; 11(5) : 335-342.
- Lippiello L, Han MS, Henderson T. Vet Therapeutics 2002 ; 2(3) : 128-135.
- Lippiello L, Hammad T. Proceedings . Am Acad Ortho Surg 2000 ; 346.
- MacLeod A, Turner T, Lennox T, Ferguson S. Compend Contin Educ Pract Vet, 2001 ; 23(9) : 842-847.
- Martel-Pelletier J, Farran A, Montell E, et al. Molecules 2015 ; 20, 4277-4289
- McIlwraith W, moderator. Compend : Equine Ed 2008 ; 3(2A) : 1-16.
- McNamara PS, Barr SC, Erb HN, Barlow LL. Vet Therapeutics 2000 ; 1(2) : 108-117.
- McNamara PS, Barr SC, Erb HN. Am J Vet Res 1996 ; 57(9) : 1390-1394.
- Millis D, moderator. Vet Forum 2007 ; 24(8A) : 1-12.
- Navarro RA. Orthop Spec Ed 2001 ; 7(2) : 1-4.
- Neil D, Caron JP, Orth MW. JAVMA 2005 ; 226(7) : 1079-1088.
- O’Grady CP, Marwin SE, Grande DA. Proceedings . AAOS 68th Annual Meeting 2001 ; paper #157.
- Orth MW, Chan PS. Workbook . AAEP Focus on Joints Conference 2004 ; 192-199.
- Pelletier JP, Raynauld JP, Beaulieu AD, et al. Arthritis Research & Therapy 2016 ; 18 : 256
- Phan PV, Au RY, Au AY, et al. Proceedings. 34th Annual Conference Veterinary Orthopedic Society 2007 ; 27.
- Phan PV, Au RY, Grzanna M, et al. Proceedings. 33rd Annual Conference Veterinary Orthopedic Society 2006 ; 118.
- Phan PV, Au R, Grzanna M, et al. 52nd Annual Meeting of the Orthopaedic Research Society, Chicago, Mar. 19-22, 2006, poster.
- Phan PV, Au RY, Grzanna M, et al. J Vet Intern Med 2006 ; 20(3) : 769.
- Phan PV, Au RY, Grzanna M, et al. J Vet Intern Med 2006 ; 20(3) : 769.
- Sauvé F, Paradis M, Refsal KR, et al. Can Vet J 2003 ; 44 : 474-479.
- Schenck RC, Clare DJ, Gilley JS, et al. Ortho Tech Rev 2000 ; 2(7) : 12-15.
- Scroggie DA, Albright A, Harris MD. Arch Intern Med 2003 ; 163 : 1587-1590.
- Stewart JD, Hulse D, Sekiya JK, Athansiou KA. Annual Meeting Virginia Ortho Soc 2003, oral presentation.
- Van Blitterswijk WJ, van de Nes JCM, Wuisman PI. BMC Complement Altern Med 2003 ; 3(1) : 2.
- Verges J, Castaneda-Hernandez G. Proceedings .West Pharmacol Soc2004 ; 47 : 50-53.
- Way W, Gibson K, Breite A. J Liq Chrom & Rel Technol 2000 ; 23(18) : 2861-2871.
- Way W, Gibson K, Breite A. J Liq Chrom & Rel Technol 2000 ; 23(18) : 2851-2860.
- Wildi LM, Raynauld JP, Martel-Pelletier J, et al. Ann Rheum Dis 2011 ; 70: 982-989
- Williams A, Gillis A, McKenzie C, et al. AJR Am J Roentgenol 2004 ; 182 : 167-172.